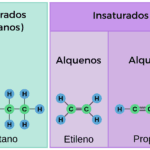
✅ Los hidrocarburos saturados normales, o alcanos lineales, se nombran usando prefijos numéricos griegos y terminan en «-ano»: metano, etano, propano, etc.
Los hidrocarburos saturados normales o lineales, también conocidos como alcanos, se nombran siguiendo una serie de reglas establecidas por la nomenclatura IUPAC (Unión Internacional de Química Pura y Aplicada). Estos compuestos se caracterizan por tener exclusivamente enlaces simples entre sus átomos de carbono y adoptar una estructura lineal sin ramificaciones.
Para nombrar los alcanos lineales, se utiliza un prefijo que indica el número de átomos de carbono seguido del sufijo «-ano». A continuación, se detallan las reglas y ejemplos para nombrar estos compuestos:
Reglas para nombrar alcanos lineales
- Identificación de la cadena principal: La cadena más larga de átomos de carbono se toma como la cadena principal.
- Uso de prefijos numéricos: Los prefijos se basan en el número de átomos de carbono en la cadena principal:
- 1 átomo de carbono: Met-
- 2 átomos de carbono: Et-
- 3 átomos de carbono: Prop-
- 4 átomos de carbono: But-
- 5 átomos de carbono: Pent-
- 6 átomos de carbono: Hex-
- 7 átomos de carbono: Hept-
- 8 átomos de carbono: Oct-
- 9 átomos de carbono: Non-
- 10 átomos de carbono: Dec-
- Adición del sufijo: Al prefijo correspondiente al número de átomos de carbono se le añade el sufijo «-ano» para formar el nombre del alcano.
Ejemplos de nombres de alcanos lineales
A continuación, se presentan algunos ejemplos de alcanos lineales con sus respectivos nombres según la nomenclatura IUPAC:
| Número de átomos de carbono | Fórmula molecular | Nombre IUPAC |
|---|---|---|
| 1 | CH4 | Metano |
| 2 | C2H6 | Etano |
| 3 | C3H8 | Propano |
| 4 | C4H10 | Butano |
| 5 | C5H12 | Pentano |
Estos son solo algunos ejemplos básicos, pero el mismo principio se aplica a alcanos con un mayor número de átomos de carbono. Para cadenas más largas, simplemente se continúa utilizando el prefijo numérico correspondiente seguido del sufijo «-ano».
Es importante señalar que estos compuestos son fundamentales en la química orgánica y tienen una amplia variedad de aplicaciones en la industria, desde combustibles hasta plásticos y productos químicos.
Principios básicos de la nomenclatura de alcanos lineales
Los alcanos lineales, también conocidos como hidrocarburos saturados normales, son compuestos orgánicos formados únicamente por átomos de carbono e hidrógeno. Estos compuestos siguen una serie de principios básicos de nomenclatura que son esenciales para su correcta identificación y clasificación.
Reglas de nomenclatura para los alcanos lineales
- Identificar la cadena más larga: La cadena principal de átomos de carbono es la más larga posible. Esta cadena determinará el nombre base del alcano.
- Numeración de la cadena: Numerar los átomos de carbono en la cadena principal empezando por el extremo más cercano a cualquier sustituyente, si es que lo hay.
- Nombrar los sustituyentes: Los grupos que cuelgan de la cadena principal se nombran como radicales alquilo. Ejemplo: metil, etil, propil.
- Combinación del nombre: Los nombres de los sustituyentes se colocan en orden alfabético, precediendo al nombre del alcano principal. Se utiliza un número para indicar la posición de cada sustituyente.
Por ejemplo, consideremos el compuesto 2-metilbutano:
- La cadena principal es de 4 carbonos: butano.
- Hay un grupo metil en el segundo carbono.
- El nombre final es 2-metilbutano.
Ejemplos de alcanos lineales
| Fórmula | Nombre | Punto de ebullición (°C) |
|---|---|---|
| CH4 | Metano | -161.5 |
| C2H6 | Etano | -88.5 |
| C3H8 | Propano | -42.1 |
| C4H10 | Butano | -0.5 |
Consejos prácticos para la nomenclatura
- Si hay más de un sustituyente, utiliza prefijos como di-, tri-, tetra-, etc. Ejemplo: 2,3-dimetilpentano.
- Para cadenas largas, es útil dibujar la estructura y numerar los carbonos antes de asignar nombres.
- Recuerda que la cadena más larga debe incluir el mayor número de sustituyentes posibles.
Estadísticas y datos relevantes
Según estudios recientes, los alcanos lineales tienen una gran importancia en la industria petroquímica. Por ejemplo, el propano y el butano se utilizan comúnmente en combustibles y como gases licuados del petróleo (GLP), representando aproximadamente el 70% del consumo de GLP en el mundo.
Casos de estudio
Un estudio realizado en 2022 mostró que el uso de butano en la producción de plásticos y productos químicos ha aumentado un 15% en los últimos cinco años, destacando la relevancia económica de los alcanos lineales en la industria.
Con estos principios básicos y ejemplos, la nomenclatura de alcanos lineales se vuelve más clara y sistemática, facilitando la comunicación y el estudio de estos importantes compuestos orgánicos.
Ejemplos prácticos de nombres de alcanos lineales
Los alcanos lineales, también conocidos como hidrocarburos saturados, son compuestos orgánicos formados exclusivamente por átomos de carbono e hidrógeno. A continuación, presentamos algunos ejemplos prácticos para ayudar a entender cómo se nombran estos compuestos.
Metano (CH4)
El metano es el alcano más simple y su fórmula molecular es CH4. Es un gas incoloro y es el principal componente del gas natural.
Etano (C2H6)
El siguiente en la serie es el etano, con una fórmula molecular de C2H6. Al igual que el metano, es un gas a temperatura ambiente. Se utiliza principalmente como combustible y en la producción de productos químicos.
Propano (C3H8)
El propano es un alcano con tres átomos de carbono y su fórmula molecular es C3H8. Es ampliamente utilizado como combustible para calefacción y en barbacoas.
Butano (C4H10)
El butano tiene cuatro átomos de carbono en su cadena y una fórmula molecular de C4H10. Es comúnmente usado en encendedores y como combustible de camping.
Tabla Comparativa de Alcanos Lineales
| Nombre | Fórmula Molecular | Usos Comunes |
|---|---|---|
| Metano | CH4 | Gas natural, producción de energía |
| Etano | C2H6 | Combustible, producción de etileno |
| Propano | C3H8 | Combustible para calefacción, barbacoas |
| Butano | C4H10 | Combustible de camping, encendedores |
Consejos Prácticos para Nombrar Alcanos
- El nombre de un alcano lineal siempre termina en «-ano».
- El prefijo indica el número de átomos de carbono en la cadena principal (por ejemplo, met- para uno, et- para dos, prop- para tres).
- Es útil memorizar los primeros cuatro nombres (metano, etano, propano y butano) ya que son los más comunes.
- Para cadenas más largas, los prefijos griegos se utilizan (por ejemplo, pent- para cinco, hex- para seis).
Dominar el nombramiento de los alcanos lineales es esencial para cualquier estudiante de química y profesional en el campo. Con la práctica y la familiarización con los prefijos y sufijos, nombrar estos compuestos se convierte en una tarea sencilla.
Preguntas frecuentes
¿Qué son los hidrocarburos saturados?
Los hidrocarburos saturados son compuestos orgánicos formados únicamente por átomos de carbono e hidrógeno unidos mediante enlaces simples.
¿Qué son los hidrocarburos normales o lineales?
Los hidrocarburos normales o lineales son aquellos que presentan una estructura lineal, es decir, los átomos de carbono están unidos en una cadena sin ramificaciones.
¿Cómo se nombran los hidrocarburos saturados normales o lineales?
Los hidrocarburos saturados normales se nombran utilizando la nomenclatura IUPAC, que consiste en indicar el número de átomos de carbono en la cadena principal y añadir el sufijo «-ano» al final.
¿Cuál es la fórmula general de los hidrocarburos saturados?
La fórmula general de los hidrocarburos saturados es CnH2n+2, donde «n» representa el número de átomos de carbono en la cadena.
¿Qué propiedades físicas suelen tener los hidrocarburos saturados?
Los hidrocarburos saturados suelen presentar puntos de ebullición y fusión más altos que los hidrocarburos insaturados, debido a la mayor fuerza de los enlaces simples entre átomos de carbono.
| Aspectos clave sobre los hidrocarburos saturados: |
|---|
| Formados por átomos de carbono e hidrógeno. |
| Enlaces simples entre átomos de carbono. |
| Se nombran según la nomenclatura IUPAC. |
| Fórmula general: CnH2n+2. |
| Propiedades físicas como puntos de ebullición y fusión más altos. |
¡Déjanos tus comentarios y revisa otros artículos relacionados con la química de los hidrocarburos en nuestra web!