✅ El carbono puede formar hasta 4 enlaces covalentes, lo que lo hace esencial en la química orgánica y la vida. ¡Descubre su versatilidad aquí!
El carbono puede formar cuatro enlaces covalentes con otros átomos. Esta capacidad única se debe a su configuración electrónica, que le permite compartir electrones con hasta cuatro átomos diferentes, lo que lo convierte en un elemento fundamental en la química orgánica y la base de la vida tal como la conocemos.
El carbono, con su número atómico 6, tiene una configuración electrónica de 1s2 2s2 2p2. Esto significa que tiene cuatro electrones de valencia disponibles para formar enlaces. La posibilidad de formar cuatro enlaces se debe a la hibridación de sus orbitales, lo que le permite crear estructuras muy diversas y complejas. A continuación, exploraremos en detalle cómo el carbono puede formar diferentes tipos de enlaces y cómo esta versatilidad se refleja en la diversidad de compuestos orgánicos.
Tipos de Enlaces que Puede Formar el Carbono
El carbono puede formar diferentes tipos de enlaces covalentes, incluyendo:
- Enlaces simples (sigma, σ): Un enlace simple se forma cuando dos átomos comparten un par de electrones. En el caso del carbono, cada enlace simple está compuesto por un enlace sigma.
- Enlaces dobles (pi, π): Un enlace doble se forma cuando dos átomos comparten dos pares de electrones. Esto incluye un enlace sigma y un enlace pi.
- Enlaces triples: Un enlace triple se forma cuando dos átomos comparten tres pares de electrones, incluyendo un enlace sigma y dos enlaces pi.
Ejemplos de Compuestos Orgánicos
La capacidad del carbono para formar cuatro enlaces se refleja en la diversidad de compuestos orgánicos que existen. Algunos ejemplos incluyen:
- Metano (CH4): El metano es el hidrocarburo más simple, donde el carbono forma cuatro enlaces simples con átomos de hidrógeno.
- Etano (C2H6): En el etano, dos átomos de carbono están unidos por un enlace simple, y cada carbono está unido a tres átomos de hidrógeno.
- Etileno (C2H4): El etileno tiene un enlace doble entre los dos átomos de carbono, y cada carbono está unido a dos átomos de hidrógeno.
- Acetileno (C2H2): El acetileno presenta un enlace triple entre los dos átomos de carbono, y cada carbono está unido a un átomo de hidrógeno.
Importancia del Carbono en la Vida
La capacidad del carbono para formar cuatro enlaces es crucial para la existencia de la vida. Esto permite la formación de una increíble variedad de moléculas orgánicas, desde simples hidrocarburos hasta complejas biomoléculas como proteínas, ácidos nucleicos y carbohidratos. La versatilidad del carbono es lo que permite la diversidad estructural y funcional de las moléculas biológicas.
Entender cómo el carbono forma enlaces y la variedad de estructuras que puede crear es fundamental para el estudio de la química orgánica y la biología molecular. Esta propiedad del carbono no solo es esencial para la estructura de las moléculas biológicas, sino también para la síntesis de nuevos materiales y compuestos en la química industrial.
Estructura electrónica del carbono y su capacidad de enlace
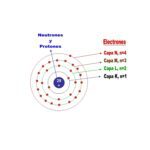
El carbono es un elemento químico fundamental, presente en todas las formas de vida conocidas. Su número atómico es el 6, lo que significa que tiene seis protones en su núcleo y, en un estado neutro, también seis electrones orbitando alrededor de este. La disposición de estos electrones en capas específicas determina sus propiedades químicas y su capacidad para formar enlaces.
Configuración Electrónica
La configuración electrónica del carbono se representa como 1s² 2s² 2p². Esto indica que:
- Los primeros dos electrones se encuentran en el orbital 1s.
- Los siguientes dos electrones ocupan el orbital 2s.
- Los últimos dos electrones están en los orbitales 2p.
Capacidad de Enlace
La capacidad del carbono para formar enlaces se deriva de su habilidad para compartir electrones y completar su capa de valencia. En su estado fundamental, el carbono tiene cuatro electrones en su capa de valencia (2s² 2p²). Esto le permite formar hasta cuatro enlaces covalentes con otros átomos.
Un ejemplo clásico de la versatilidad del carbono es el metano (CH₄), donde el carbono forma cuatro enlaces simples con cuatro átomos de hidrógeno. Esta capacidad para formar múltiples enlaces covalentes es lo que hace al carbono tan esencial en la química orgánica.
Geometría Molecular
La geometría de las moléculas de carbono también es crucial para entender sus propiedades. Algunas de las geometrías más comunes incluyen:
- Tetraédrica: Como en el metano (CH₄), donde los cuatro enlaces del carbono están dirigidos hacia los vértices de un tetraedro.
- Trigonal plana: Como en el etileno (C₂H₄), donde el carbono forma un doble enlace con otro carbono y enlaces simples con otros átomos, creando una estructura plana.
- Lineal: Como en el acetileno (C₂H₂), donde el carbono forma un triple enlace con otro carbono y enlaces simples con átomos de hidrógeno, resultando en una estructura lineal.
Hibridación
El concepto de hibridación es esencial para entender cómo el carbono forma diferentes tipos de enlaces y geometrías. Algunos tipos de hibridación incluyen:
- sp³: En moléculas como el metano, donde el carbono tiene cuatro enlaces simples.
- sp²: En moléculas como el etileno, donde el carbono forma un doble enlace.
- sp: En moléculas como el acetileno, donde el carbono forma un triple enlace.
Estas hibridaciones afectan la energía y la geometría de las moléculas, permitiendo al carbono formar una variedad de estructuras complejas y estables.
Casos de Estudio
Para ilustrar la importancia de la capacidad de enlace del carbono, consideremos algunos casos de estudio:
- Grafito: El carbono forma una estructura en capas, donde cada átomo está unido a tres átomos de carbono en un plano, dejando un electrón libre para conducir electricidad.
- Diamante: Cada átomo de carbono forma enlaces con cuatro átomos de carbono en una estructura tetraédrica, resultando en una de las sustancias más duras conocidas.
Estos ejemplos destacan cómo la estructura electrónica y la capacidad de enlace del carbono permiten la formación de materiales con propiedades físicas y químicas únicas.
Tipos de enlaces que puede formar el carbono
El carbono es un elemento versátil y puede formar distintos tipos de enlaces, lo cual lo hace fundamental en la química orgánica. A continuación, exploraremos los diferentes tipos de enlaces químicos que puede formar el carbono.
1. Enlaces sencillos (sigma)
Los enlaces sencillos o sigma son los más comunes y se forman cuando dos átomos de carbono comparten un par de electrones. Este tipo de enlace es más fuerte y estable debido a la superposición directa de los orbitales.
- Ejemplo: En el etano (C2H6), cada átomo de carbono está unido a tres átomos de hidrógeno y a otro átomo de carbono mediante enlaces sencillos.
2. Enlaces dobles (pi)
Los enlaces dobles consisten en un enlace sigma y un enlace pi, que se forma por la superposición lateral de los orbitales p. Este tipo de enlace es menos fuerte que un enlace sigma, pero proporciona mayor rigidez a la molécula.
- Ejemplo: En el etileno (C2H4), los dos átomos de carbono están unidos por un enlace doble, lo que restringe la rotación alrededor del enlace.
3. Enlaces triples
Un enlace triple está compuesto por un enlace sigma y dos enlaces pi. Estos enlaces son los más fuertes y cortos entre los átomos de carbono, pero también son menos flexibles.
- Ejemplo: En el acetileno (C2H2), los dos átomos de carbono están unidos por un enlace triple, lo que resulta en una molécula lineal.
4. Enlaces aromáticos
Los enlaces aromáticos se encuentran en compuestos que tienen estructuras cíclicas con enlaces conjugados, como el benceno. Estos enlaces son únicos porque los electrones se deslocalizan sobre la estructura, proporcionando estabilidad adicional.
- Ejemplo: En el benceno (C6H6), los átomos de carbono forman un anillo con enlaces simples y dobles alternados, lo que resulta en una estructura altamente estable.
Comparación de tipos de enlaces
| Tipo de Enlace | Fuerza | Longitud | Flexibilidad |
|---|---|---|---|
| Enlace sencillo (sigma) | Media | Larga | Alta |
| Enlace doble (pi) | Alta | Media | Media |
| Enlace triple | Muy alta | Corta | Baja |
| Enlace aromático | Alta | Media | Alta |
La capacidad del carbono para formar estos diversos tipos de enlaces lo convierte en un elemento clave en la formación de una amplia variedad de compuestos, desde simples hidrocarburos hasta complejas macromoléculas biológicas.
Preguntas frecuentes
¿Cuántos enlaces puede formar un átomo de carbono?
Un átomo de carbono puede formar hasta 4 enlaces covalentes.
¿Qué tipo de enlaces forma el carbono en compuestos orgánicos?
El carbono forma principalmente enlaces covalentes en compuestos orgánicos.
¿Por qué el carbono es el elemento base de la química orgánica?
El carbono es versátil en la formación de enlaces y puede unirse consigo mismo y con otros elementos, lo que le permite formar una amplia variedad de compuestos.
¿Cuál es la importancia del carbono en los seres vivos?
El carbono es esencial en las biomoléculas como proteínas, ácidos nucleicos, carbohidratos y lípidos, que son fundamentales para la vida.
| Puntos clave sobre el carbono |
|---|
| El carbono tiene 6 electrones y 6 protones en su núcleo. |
| El carbono puede formar enlaces simples, dobles o triples con otros átomos de carbono u otros elementos. |
| Los enlaces covalentes del carbono pueden ser polares o no polares. |
| El carbono es la base de la química orgánica debido a su capacidad de formar cadenas largas y ramificadas. |
| Los compuestos de carbono son fundamentales en la industria, la medicina, la alimentación y la biotecnología. |
¡Déjanos tus comentarios y no olvides revisar otros artículos relacionados con la química orgánica en nuestra web!