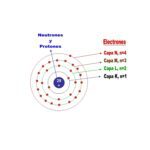
✅ El grupo IV A incluye carbono, silicio, germanio, estaño y plomo. Son esenciales en tecnología y la vida; tienen 4 electrones de valencia.
El grupo IV A de la tabla periódica, también conocido como el grupo del carbono, está compuesto por los elementos carbono (C), silicio (Si), germanio (Ge), estaño (Sn) y plomo (Pb). Estos elementos comparten ciertas características y propiedades debido a su configuración electrónica similar, que les permite comportarse de manera análoga en varias reacciones químicas y aplicaciones industriales.
A continuación, exploraremos en detalle las características del grupo IV A de la tabla periódica, analizando sus propiedades físicas y químicas, así como su importancia en diversas aplicaciones.
Propiedades Físicas
- Estados de la Materia: En este grupo, el carbono es un no metal, el silicio y el germanio son metaloides, y el estaño y el plomo son metales. Esto muestra una transición de no metal a metal dentro del mismo grupo.
- Puntos de Fusión y Ebullición: Los puntos de fusión y ebullición tienden a disminuir al descender en el grupo. Por ejemplo, el carbono tiene uno de los puntos de fusión más altos entre los elementos (sublima a 3915 K), mientras que el plomo tiene un punto de fusión relativamente bajo (600.61 K).
- Estructura Cristalina: El carbono puede existir en varias formas alotrópicas, incluyendo el diamante y el grafito, que tienen estructuras cristalinas muy diferentes. El silicio y el germanio cristalizan en la estructura del diamante. El estaño tiene dos formas alotrópicas: el estaño blanco (beta) y el estaño gris (alfa).
Propiedades Químicas
- Configuración Electrónica: Todos los elementos del grupo IV A tienen una configuración electrónica que termina en ns2np2, lo que les da cuatro electrones de valencia.
- Estados de Oxidación: El estado de oxidación más común para estos elementos es +4. Sin embargo, el carbono también puede mostrar un estado de oxidación de -4 (como en el metano, CH4). A medida que se desciende en el grupo, los estados de oxidación +2 se vuelven más comunes debido al efecto inerte del par de electrones.
- Reactividad: La reactividad varía considerablemente dentro del grupo. El carbono es relativamente no reactivo a temperatura ambiente, mientras que el plomo puede reaccionar fácilmente con ácidos y bases.
Aplicaciones de los Elementos del Grupo IV A
- Carbono: Utilizado en la fabricación de compuestos orgánicos, combustibles fósiles, y materiales avanzados como el grafeno.
- Silicio: Fundamental en la industria de semiconductores y la fabricación de dispositivos electrónicos.
- Germanio: Utilizado en electrónica y en la fabricación de fibras ópticas y lentes infrarrojas.
- Estaño: Empleado en aleaciones como el bronce y en recubrimientos protectores para otros metales.
- Plomo: Utilizado en baterías de plomo-ácido, aunque su uso está siendo reducido debido a problemas de toxicidad.
La comprensión de las propiedades y aplicaciones de los elementos del grupo IV A es esencial para diversas disciplinas científicas y tecnológicas. Estos elementos desempeñan roles cruciales en la química orgánica, la electrónica, la metalurgia y otros campos importantes.
Propiedades físicas de los elementos del grupo IV A
Los elementos del grupo IV A de la tabla periódica incluyen carbono (C), silicio (Si), germanio (Ge), estaño (Sn) y plomo (Pb). Estos elementos presentan una variedad de propiedades físicas interesantes que cambian de manera significativa a medida que descendemos en el grupo.
Estados de Agregación
Mientras que el carbono puede encontrarse en formas sólidas como el diamante y el grafito, el silicio, germanio, estaño y plomo son todos sólidos a temperatura ambiente. Esta diversidad en las formas del carbono es un indicador de su versatilidad y importancia en la naturaleza.
Puntos de Fusión y Ebullición
- Carbono: El punto de fusión del diamante es de aproximadamente 3550°C, uno de los más altos entre los elementos.
- Silicio: Tiene un punto de fusión de 1414°C y un punto de ebullición de 3265°C.
- Germanio: Su punto de fusión es de 938°C y el de ebullición es de 2833°C.
- Estaño: Presenta un punto de fusión de 231.9°C y un punto de ebullición de 2602°C.
- Plomo: Tiene un punto de fusión de 327.5°C y un punto de ebullición de 1749°C.
Densidad
La densidad de estos elementos varía considerablemente:
- Carbono: En su forma de grafito, la densidad es aproximadamente 2.267 g/cm³, mientras que en forma de diamante es 3.515 g/cm³.
- Silicio: Tiene una densidad de 2.33 g/cm³.
- Germanio: Su densidad es de 5.323 g/cm³.
- Estaño: La densidad es de 7.31 g/cm³.
- Plomo: Tiene una densidad de 11.34 g/cm³.
Estructura Cristalina
La estructura cristalina de estos elementos también varía:
- Carbono: El diamante tiene una estructura cúbica centrada en las caras, mientras que el grafito tiene una estructura hexagonal.
- Silicio y Germanio: Ambos poseen una estructura cúbica centrada en las caras similar a la del diamante.
- Estaño: Puede encontrarse en dos formas alotrópicas: estaño gris (estructura cúbica) y estaño blanco (estructura tetragonal).
- Plomo: Tiene una estructura cúbica centrada en las caras.
Consejos Prácticos para el Manejo de Estos Elementos
Al trabajar con estos elementos, es crucial tener en cuenta ciertas precauciones:
- El plomo es tóxico y debe manejarse con cuidado, utilizando siempre equipo de protección.
- El silicio y el germanio son fundamentales en la industria electrónica, por lo que su pureza es clave para su eficacia.
- El carbono en forma de diamante y grafito tiene aplicaciones únicas, desde herramientas de corte hasta lubricantes.
Estudios Recientes
Un estudio realizado en 2021 mostró que el uso de silicio en baterías de iones de litio puede aumentar su capacidad hasta un 20% en comparación con las baterías tradicionales de grafito. Esto subraya la importancia de continuar investigando las propiedades físicas y sus aplicaciones potenciales.
Aplicaciones industriales y tecnológicas del grupo IV A
El grupo IV A de la tabla periódica incluye elementos como el carbono (C), el silicio (Si), el germanio (Ge), el estaño (Sn) y el plomo (Pb). Estos elementos juegan un papel crucial en diversas industrias y tecnologías gracias a sus propiedades únicas.
Carbono (C)
El carbono es uno de los elementos más versátiles y se encuentra en varias formas como el grafito, el diamante y los nanotubos de carbono. Sus aplicaciones incluyen:
- Materiales de construcción: El grafito se utiliza en lápices y como lubricante.
- Electrónica: Los nanotubos de carbono se usan en la fabricación de pantallas y transistores.
- Joyería: El diamante se emplea en anillos y otras joyas.
Ejemplo concreto
En la industria de la tecnología, los nanotubos de carbono han permitido avances significativos en la eficiencia de los microchips, mejorando su conductividad eléctrica y resistencia.
Silicio (Si)
El silicio es fundamental en la industria de los semiconductores y se utiliza principalmente en:
- Fabricación de chips: Es el material base para casi todos los microprocesadores y memorias RAM.
- Paneles solares: Se emplea en la producción de células fotovoltaicas para energía solar.
- Vidrios y cerámicas: Se usa en la fabricación de vidrio templado y cerámicas avanzadas.
Recomendación práctica
Para maximizar el rendimiento de los paneles solares, es crucial utilizar silicio de alta pureza y optimizar su orientación y mantenimiento.
Germanio (Ge)
El germanio es menos común pero encuentra aplicaciones en:
- Fibra óptica: Se usa en la producción de fibras ópticas debido a su baja dispersión y alta transmisión.
- Electrónica: Componentes de transistores y detectores de radiación.
- Química: Catalizadores para diversas reacciones químicas.
Estadística relevante
Según un reporte de 2021, el mercado de fibra óptica creció un 8% anual, impulsado en parte por el uso de germanio en su manufactura.
Estaño (Sn)
El estaño es muy utilizado en:
- Soldadura: Es un componente esencial en aleaciones de soldadura para electrónica.
- Recubrimientos: Se usa en el recubrimiento de otros metales para prevenir la corrosión.
- Vidrios: Producción de vidrio flotado.
Consejo práctico
Para evitar problemas de oxidación en las aleaciones de soldadura, es recomendable usar aleaciones de estaño con antioxidantes añadidos.
Plomo (Pb)
El plomo tiene varias aplicaciones aunque su uso ha disminuido debido a problemas de toxicidad:
- Baterías: Se encuentra en baterías de plomo-ácido para vehículos y sistemas de respaldo.
- Protección radiológica: Utilizado en chalecos protectores y barreras contra radiación.
- Construcción: Usado en materiales de construcción y tuberías antiguas.
Investigación reciente
Un estudio reciente ha demostrado que las baterías de plomo-ácido pueden ser recicladas eficientemente en un 98%, lo que reduce su impacto ambiental.
Comparación de aplicaciones
| Elemento | Aplicación principal | Industria |
|---|---|---|
| Carbono | Nanotubos de carbono | Tecnología |
| Silicio | Semiconductores | Electrónica |
| Germanio | Fibra óptica | Telecomunicaciones |
| Estaño | Soldadura | Electrónica |
| Plomo | Baterías | Automotriz |
Preguntas frecuentes
¿Cuáles son los elementos del grupo IV A de la tabla periódica?
Los elementos del grupo IV A son carbono (C), silicio (Si), germanio (Ge), estaño (Sn) y plomo (Pb).
¿Cuál es la valencia de los elementos del grupo IV A?
Los elementos del grupo IV A tienen una valencia de +4.
¿Cuáles son algunas aplicaciones importantes de los elementos del grupo IV A?
Algunas aplicaciones incluyen la fabricación de semiconductores en el caso del silicio, y la producción de vidrio y aleaciones en el caso del estaño.
- Los elementos del grupo IV A son conocidos como los «elementos del carbono» debido a su capacidad para formar compuestos con este elemento.
- El carbono es un elemento fundamental para la vida, ya que forma la base de las moléculas orgánicas.
- El silicio es el segundo elemento más abundante en la corteza terrestre después del oxígeno.
- El plomo es un metal pesado que puede tener efectos tóxicos en los seres vivos si se ingiere en grandes cantidades.
- El estaño se utiliza en la fabricación de latas para alimentos debido a su resistencia a la corrosión.
- El germanio se utiliza en la producción de dispositivos semiconductores y en fibra óptica.
¡Déjanos tus comentarios y revisa otros artículos de nuestra web para seguir aprendiendo sobre la tabla periódica y sus elementos!